Was ist Ozeanversauerung?
Seit Beginn der Industrialisierung hat der Ozean etwa 30 Prozent allen Kohlendioxids (CO2) aufgenommen, das durch menschliche Aktivitäten in die Atmosphäre gelangte.
Einerseits verlangsamt das Meer durch diesen unschätzbaren Service – die Wissenschaft spricht von einer Funktion als „CO2-Senke“ – den globalen Klimawandel. Gäbe es diesen natürlichen Speicher auf unserem Planeten nicht, würde er sich viel stärker und viel schneller erwärmen als wir es heute bereits feststellen. Denn Kohlendioxid ist ein gefährliches Treibhausgas: Gelangt es in die Atmosphäre, reflektiert es dort von der Erde abgestrahlte Wärme, und sie heizt sich auf.
Andererseits löst das Gas im Meer eine folgenreiche chemische Reaktion aus: Kohlensäure entsteht, und das Wasser wird saurer – sein pH-Wert sinkt. Der durchschnittliche pH-Wert der Meeresoberfläche ist im Zuge der Industrialisierung bereits von 8,2 auf 8,1 gesunken, was einem Anstieg des Säuregrads um 26 Prozent entspricht.
Mit zunehmender Versauerung sinkt die Konzentration der Karbonat-Ionen. Doch genau diese Moleküle benötigen kalkbildende Organismen wie Muscheln, Korallen oder bestimmte Plankton-Arten, um ihre Schalen und Skelette aufzubauen. Je weniger Karbonat-Ionen zur Verfügung stehen, desto aufwändiger wird die Kalkbildung. Wie groß der zusätzliche Aufwand ist, hängt zudem davon ab, welche Form des Kalziumkarbonats (Kalk) Organismen produzieren – das leichter lösliche Aragonit oder das etwas beständigere Kalzit.
Auch andere Meereslebewesen, die keine Kalkschalen oder -skelette besitzen, müssen im saureren Wasser mehr Energie aufbringen, um ihre Körperfunktionen zu regulieren. Zusätzliche Energie, die für das Überleben unter saureren Bedingungen benötigt wird, fehlt Organismen dann für ihr Wachstum, die Fortpflanzung oder den Widerstand gegen andere Umweltbelastungen.
Gleichzeitig profitieren einige Spezies von dem zusätzlichen gelösten CO2 – im Nahrungsnetz gibt es Gewinner und Verlierer.
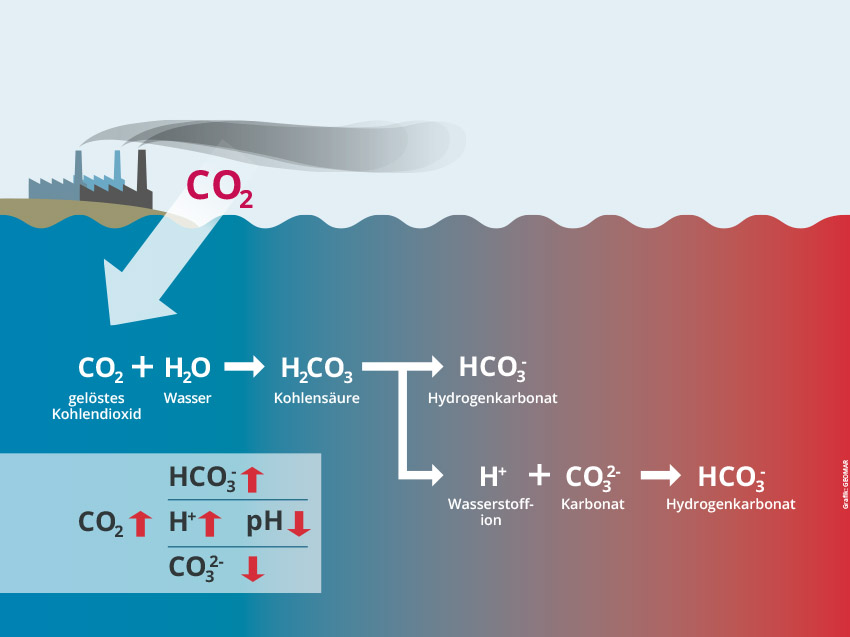
Für den Prozess der Ozeanversauerung sind zwei chemische Reaktionen besonders wichtig, die gleichzeitig ablaufen können:
Die Entstehung von Kohlensäure und die anschließende Freisetzung von Wasserstoff-Ionen:
CO2 + H2O ↔ H2CO3 ↔ H+ + HCO3–
(Kohlendioxid + Wasser ↔ Kohlensäure ↔ Wasserstoff-Ionen + Hydrogenkarbonat-Ionen)
Die Reaktion zwischen Karbonat-Ionen, CO2 und Wasser, bei der Hydrogenkarbonat-Ionen entstehen:
CO2 + H2O + CO32- 2↔ HCO3–
(Kohlendioxid + Wasser + Karbonat-Ionen ↔ Hydrogenkarbonat-Ionen)
MEHR WISSEN: Versauerung in der Arktis // Plankton // Kaltwasserkorallen // Tropische Korallen // Gesellschaftliche Folgen